La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) aprobó el primer test rápido de COVID-19 cien por ciento nacional, desarrollado en los laboratorios de la UNLP. La prueba serológica detecta anticuerpos en sangre y permite saber, en apenas cinco minutos, si una persona está o estuvo infectada con el virus SARS-CoV-2.
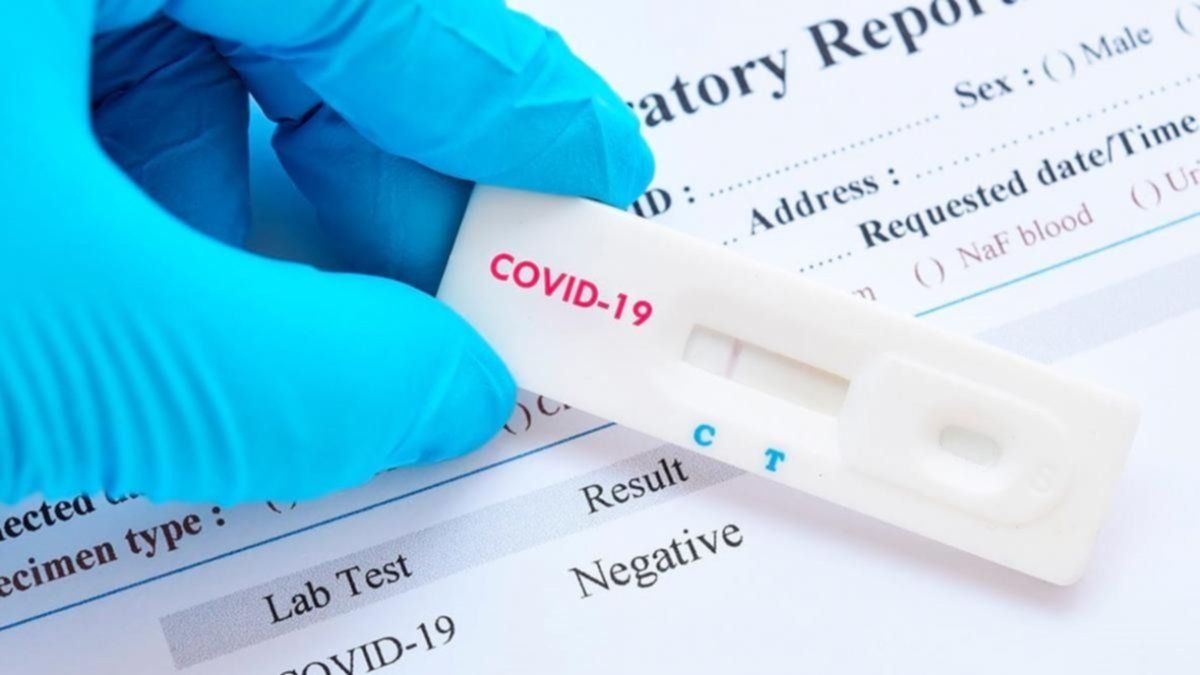
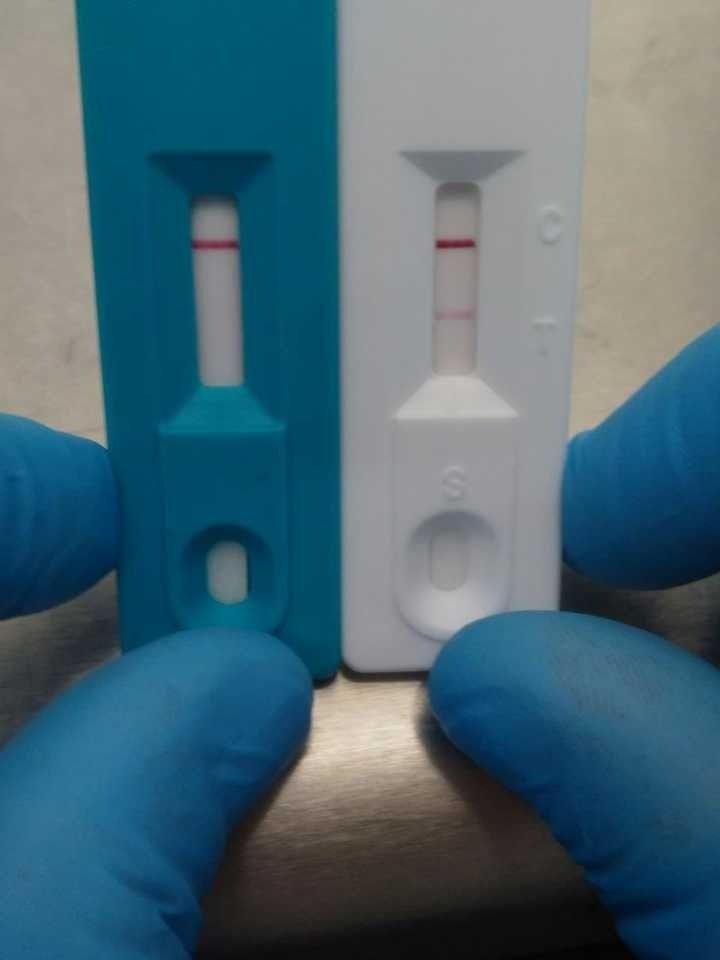
De acuerdo a los desarrolladores, el principio de este tipo de prueba de diagnóstico se basa en la detección de anticuerpos en sangre mediante un principio inmunocromatográfico y detección visual. El resultado se observa a simple vista, por aparición de líneas de color y, como ocurre con otros test que determinan anticuerpos, indican si la persona está o estuvo en infectada con el virus.
Una de las principales ventajas es que permite realizar estudios poblacionales a gran escala y desde el punto de vista epidemiológico, realizar mapeo y segregación de áreas contemplando métricas como incidencia de la enfermedad e inmunidad poblacional adquirida.
El dispositivo fue creado por especialistas del Centro de Investigación y Desarrollo en Fermentaciones Industriales (CINDEFI), con sede en la Facultad de Ciencias Exactas, dependiente de la UNLP y el CONICET. El equipo es liderado por los doctores Sebastián Cavalitto y Gastón Ortiz.
Y el propio Ortiz relató que junto a su equipo empezaron a trabajar "con la idea del proyecto a mediados de marzo, ni bien supimos que se nos venía encima esta pandemia”. “Comenzamos a pensar a ver qué tipo de solución podíamos dar y surgió este tipo de testeo que podía ayudar a la resolución de la pandemia y a partir de septiembre estábamos produciendo el piloto para enviarlos a la ANMAT. Fue un proceso tedioso y laborioso”, destacó.

En ese sentido, señaló que para obtener la aprobación del ente encargada del registro, la fiscalización, el control y la vigilancia de medicamentos. “Nosotros pudimos hacer el ensayo en más de 300 sueros analizados, entre pacientes portadores COVID. Hicimos reactividad cruzada con enfermedades endémica que es bastante importante porque eso es ver qué capacidad de reactividad cruzada tiene el test con las enfermedades que son endémicas en nuestro país como dengue, chagas y ese tipo de enfermedades”, detalló.
Al ser consultado de efectividad, Ortiz declaró que “en el caso de los test se habla de sensibilidad y especificidad. El test presenta un 91% de especificidad y un 86% de sensibilidad”. Y remarcó: “Su uso es institucional, en el prospecto del producto ANMAT hace una aprobación para uso profesional. No es de uso doméstico, no se puede comprar en una farmacia”.

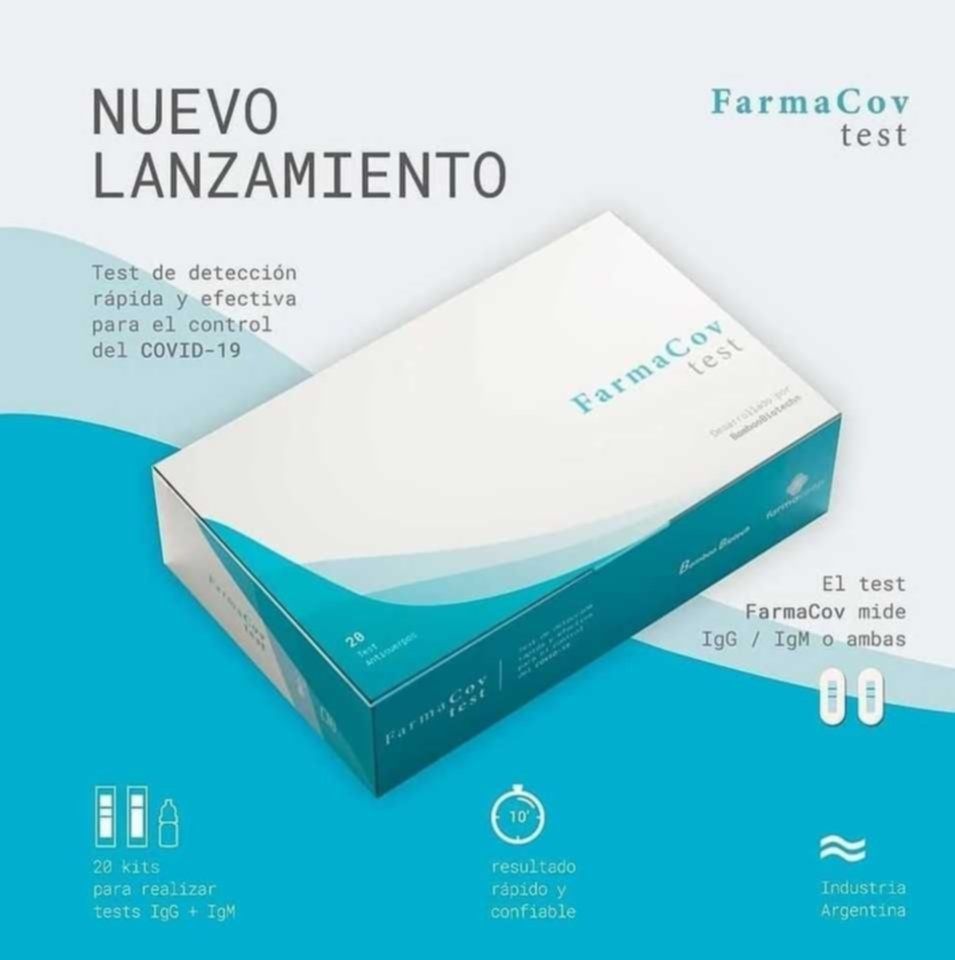
El test serológico rápido obtuvo la aprobación de la ANMAT y, en consecuencia, ya está en condiciones de ser comercializado: saldrá al mercado con el nombre de FarmaCov test y tiene un costo de 4.50 dólares. “No es diagnóstico el test pero puede ser utilizado como un síntoma más y confirmatorio con un resultado de PCR”, indicó.
En cuanto a los desafíos, el director del CINDEFI expresó, "que fue obtener financiamiento del sector privado para su realización". "Conseguimos el apoyo por parte de Bamboo Biotech SAS y Alimentos proteicos SRL, quienes realizaron el aporte de capitales necesarios para continuar adelante con el proyecto. La asociación con estas dos empresas también nos llevó a vincularnos con Farmacoop Lta que adoptó la tecnología desarrollada y es responsable de la producción de los test".

Por último, Ortiz señaló que fue una gran alegría la aprobación de la ANMAT pero reveló que todavía no tuvieron tiempo para celebrar este logro con los integrantes del equipo de investigación. “Uno sintió un alivio en poder generar el producto y que esté disponible. Eso significa un montón para nosotros”, concluyó.