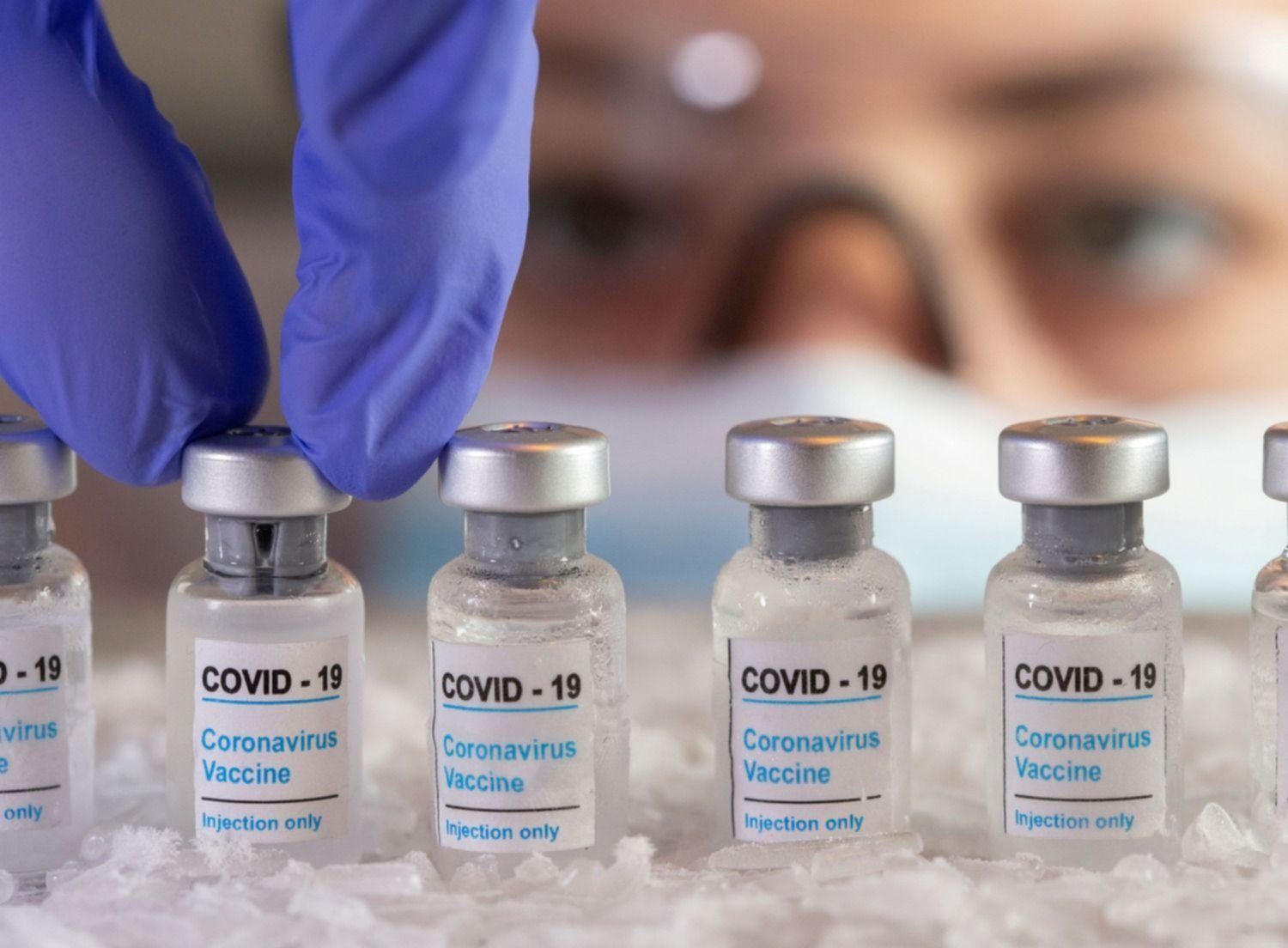
Mientras la vacunación contra el coronavirus avanza en todo el mundo, tanto Pfizer como Moderna estudian si sus vacunas pueden aplicarse en niños de 5 a 11 años, una población que aún no fue inmunizada. Por un pedido de la Administración de Medicinas y Alimentos de EEUU (FDA, por sus siglas en inglés), los laboratorios ampliaron sus investigaciones para determinar si sus inoculaciones pueden utilizarse para proteger del COVID-19 a este rango etario.
Según publicó The New York Times, varias personas familiarizadas con los ensayos dijeron que la FDA manifestó a Pfizer-BioNTech y Moderna que el tamaño y el alcance de sus estudios pediátricos, eran inadecuados para detectar los efectos secundarios raros, incluida la miocarditis, una inflamación del músculo cardíaco, y la pericarditis, una inflamación de la delgada membrana similar a un saco que rodea al corazón.
En este marco, la FDA instó a las empresas a que incluyan a 3.000 niños en el grupo de edad de 5 a 11 años, el grupo para el que se esperaban los primeros resultados. Ante la consulta del medio norteamericano, un vocero de Moderna, Ray Jordan, confirmó que la compañía tiene la intención de expandir su estudio “para inscribir una base de datos de seguridad más grande que aumenta la probabilidad de detectar eventos más raros” y espera buscar autorización de emergencia en el “invierno (estadounidense) de 2021/principios de 2022”.
Vale destacar que la vacuna de Pfizer-BioNTech es la única que hasta el momento cuenta con la autorización de emergencia para ser aplicada en adolescentes de entre 12 y 18 años, por parte de la Administración de Medicinas y Alimentos de EEUU (FDA, por sus siglas en inglés) y la Agencia Europea de Medicamentos (EMA), lo mismo que, en Argentina, por la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT). Moderna tramita que su inoculante reciba la misma aprobación.

El ensayo de Moderna comenzó a reclutar pacientes en marzo con el objetivo de inscribir a 6.795 participantes entre las edades de seis meses y menos de 12 años, al tiempo que Pfizer tiene un cronograma más rápido que Moderna y es posible que pueda cumplir con las expectativas de la FDA sobre un tamaño de prueba más grande y aun así presentar una solicitud para expandir la autorización de emergencia de su vacuna para fines de septiembre.
Por su parte, Pfizer declaró anteriormente que espera tener resultados para el grupo de 5 a 11 años en septiembre, con resultados para niños de dos a cinco años poco después. Los resultados para los niños más pequeños entre las edades de seis meses y dos años se esperan en octubre o noviembre.